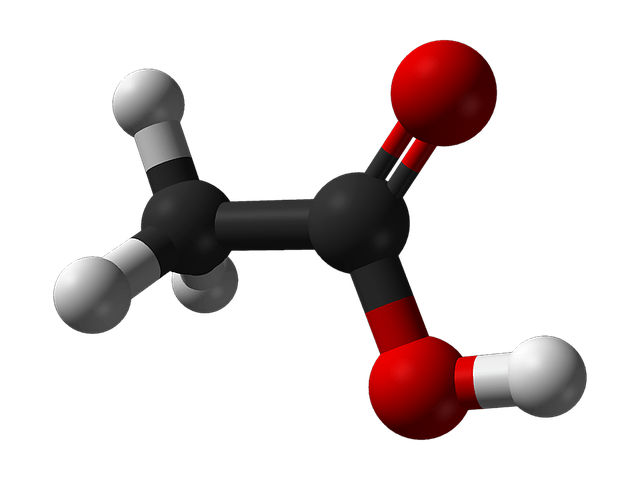
Essig- Ethansäure
Die schwache Carbonsäure „acidum aceticum“ oder Ethansäure (CH_3COOH) ist bei Raumtemeratur eine farblose, hygroskopische Flüssigkeit, mit stechendem Geruch, die brennbar ist und sich gut mit Wasser mischt. Ihre wässrigen Lösungen werden als Essig bezeichnet. Ethansäure färbt den Indikator UNITEST rot (Video Indikator)
Das Wort „Essig“ ist ursprünglich vom lateinischen Wort „acetum“ für saurer Wein abgeleitet und wurde über das mittelhochdeutsche „ezzich“ zu unserem Wort für diese Substanz.
Die heute synthetisch -also technisch- gewonnene Ethansäure wird in der Industrie zur Herstellung von Kunststoffen(Polyvinylacetat oder Celuloseacetat) genutzt. Der Jahresverbrauch liegt bei etwa 10.000.000 t.
Reine Essigsäure (99%+)erstarrt bei 16°C . Daher wird für diese reine Form oft der Begriff Eisessig verwendet.
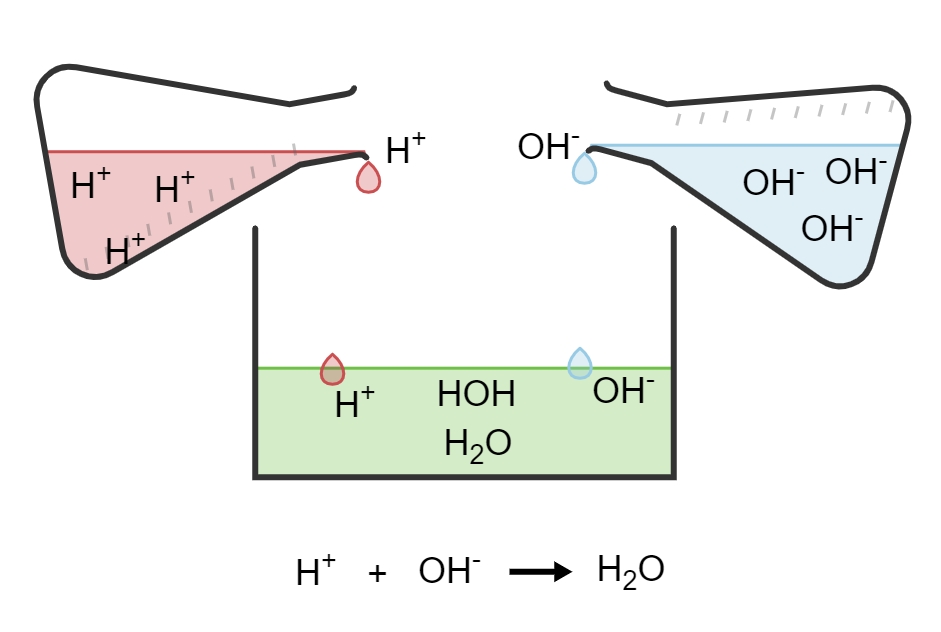
Das Molekül der Ethansäure zerfällt beim Lösen in Wasser nur wenigen Prozentanteilen in das Acetation CH_3COO^- und das Proton H^+. Es entsteht eine mittelstarke Säure, die unedle Metalle unter Wasserstoff- und Acetatsalzbildung angreift.
Schon die Römer nutzten Essig in der Küche und erzeugten daraus das alkoholfreie Erfrischungsgetränk „Posca“ und die alkoholhaltige Variante „Lora“- eine Mischung aus Essig und Wasser. Römische Soldaten tranken massenhaft Posca und machten das so verwendete Wasser -eventuell unwissend – durch die antibakterielle Wirkung des Essigs erst genießbar.
Fragt mal eure Großeltern oder Urgroßeltern nach dem Erfrischungsgetränk ihrer Jugend!
Sie werden Essig erwähnen…
Speiseessig kaufen wir heute als ca. 5%-igen Tafelessig(Wasseranteil 95%) oder als 25% -ige Essig-Essenz (Wasseranteil 75%). Er wurde und wird in der Küche – Lebensmittelzusatzstoff: E 260 – als Würze oder Konservierungsmittel und auch im Bad als Reiniger verwendet. Der leicht ätzende Essig wirkt dabei gegen Kalkverunreinigungen genauso wie gegen die Außenhülle von Bakterien oder Pilzen(Schimmel).
Woraus entsteht eigentlich Essig?
Hier einige Haushaltstricks zu Essig…
![]()