Stöchiometrie Übungen (m/m)
Die Aufgabensammlung Stöchiometrie mit 10 Masse/Masse Aufgaben und ihre Lösungen.
Sollte ich mich doch irgendwo verrechnet haben, bitte ich um einen kleinen Tipp…
Aufrufe 22722 total views , Heute 1 views today
Chemie kann man üben!

Die Aufgabensammlung Stöchiometrie mit 10 Masse/Masse Aufgaben und ihre Lösungen.
Sollte ich mich doch irgendwo verrechnet haben, bitte ich um einen kleinen Tipp…
Aufrufe 22722 total views , Heute 1 views today
Zum Verständnis solltest Du Dich unbedingt vorher mit der Avogadrokonstante
beschäftigt haben und wissen, was sie Stoffmenge (n) ist.
Dank Herrn Loschmidt wissen wir :
„22,4 Liter Gas enthalten immer ein Mol dieser gasförmigen Substanz.“
So ergibt sich die Frage, nach einer Sammlung dieser Informationen.
Jemand müsste die Substanzen der Welt verdampfen und 22,4 Liter der idealen Gase wiegen.
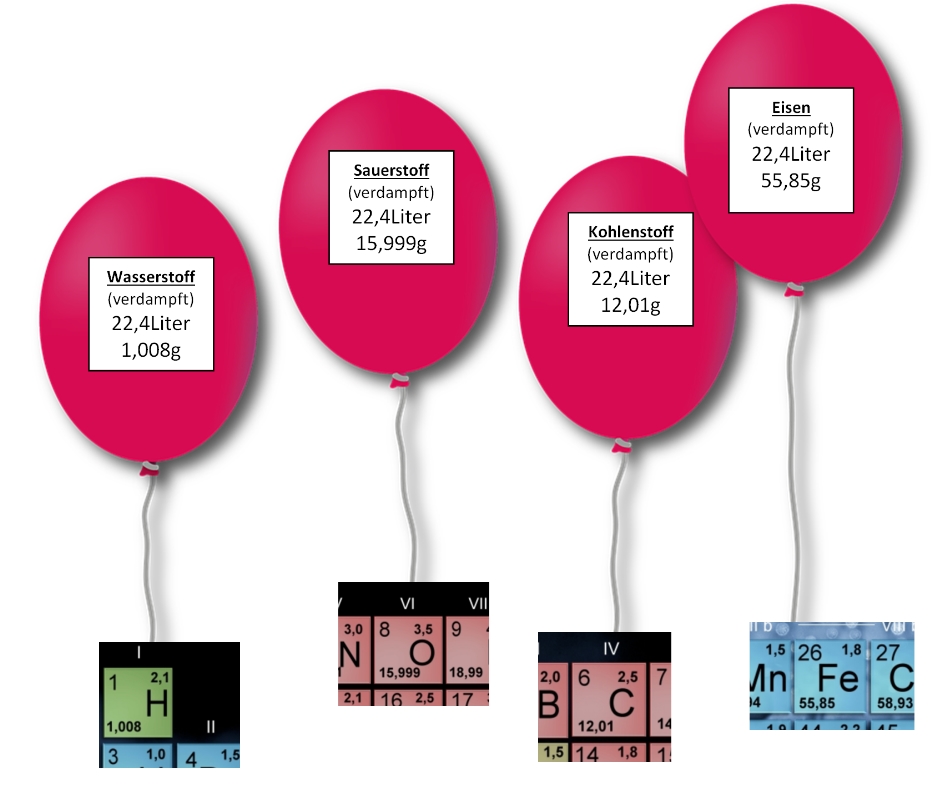
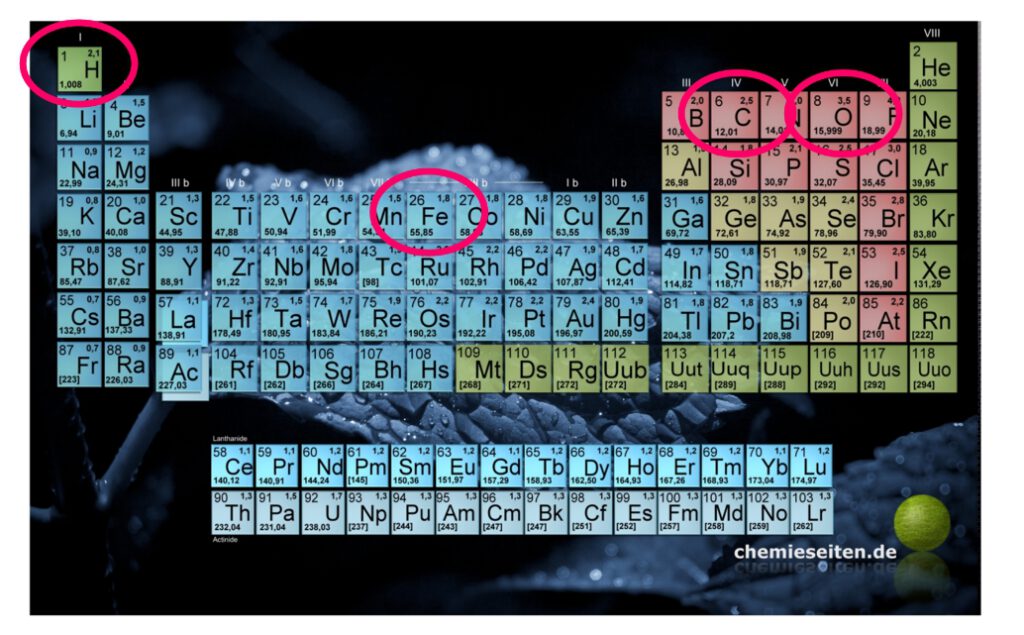
Diese Masse eines Mols einer Substanz nennt man die molare Masse M [g/mol]
Man findet diese Angabe für alle Elemente als relative Atommasse im PSE!
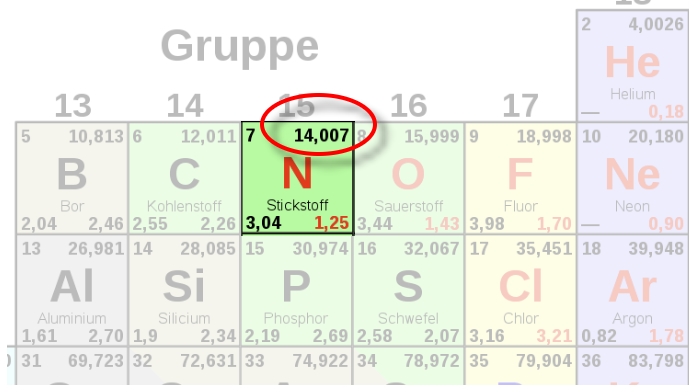
1 mol Stickstoffatome [ 7N ] wiegen also 14,007 g
(Uns reicht die gerundete Zahl ohne Kommastellen zum Rechnen)
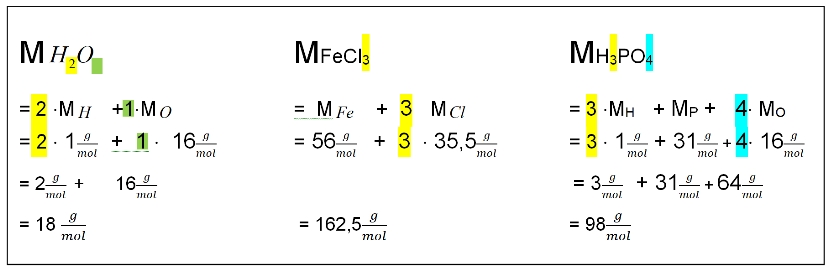
Für alle wichtigen Verbindungen kann man die Molare Masse im Tafelwerk nachschauen!
Die molaren Massen aller weiteren Substanzen muss man errechnen:
Die Formel der Stoffe ist dafür die Berechnungsvorschrift:
Aufrufe 6716 total views
Benachrichtigungen