Atombau – Unterrichtsfilm
Variante 1
Variante 2:
![]()
Chemie kann man üben!

Variante 1
Variante 2:
![]()

Der neuseeländische Baron war ein herausragender Experimentalphysiker mit sehr systemischer Denkweise,
der 1908 den Nobelpreis für Chemie erhielt. Rutherford definierte die Halbwertszeit, katalogisierte
die Strahlungsarten und stellte die Hypothese aus, dass Elemente durch Strahlung in Elemente mit
niedrigerer Ordnungszahl zerfallen.
Sein bekanntester Beitrag aber war der Streuversuch, mit dem Rutherford nachwies, dass Atome keine Materie
gefüllte Teilchen sind.
Rutherfords Streuversuch:
Eine weitere Variante bei youtube.de schauen.
Das Kern-Hülle-Modell war geboren.
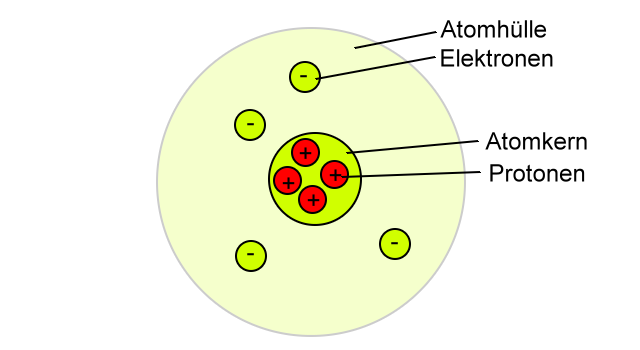
Die Atome sind keine materiegefüllten Kugeln!
Sie bestehen aus einem positiv geladenen Atomkern(Kern), der positiv geladene Protonen beherbergt und einer fast leeren riesigen Atomhülle, in der die negativ geladenen Elektronen (entdeckt 1897 von Thomson und Wiechert)
Rutherford konnte zur Ordnung und Bewegungen der Elektronen noch keine Aussagen machen.
Das Neutron als Bestandteil des Kerns war noch unbekannt. Aber Rutherford sagte seine Existenz selbst noch 1932 voraus.
![]()
![]()
Arbeitsmaterial:
Geschichte des PSE (Broschüre der GdCh)
Die Suche nach den Bausteinen unserer Welt
In Darmstadt (Deutschland) wurde und wird auch heute noch nach den Bausteinen des Universums gesucht. Hier entdeckte man Elemente durch ein fantastisches Experiment in einem Teilchenbeschleuniger.
Welche Informationen man im PSE findet und wozu man diese nutzt erfahrt ihr hier …
Einen sehr schön gestalteten Kurs „PSE“ findet man auch bei Studiflix.de. LiNK
![]()